بی کربنات سدیم چیست؟ همه چیز درباره جوش شیرین Sodium Bicarbonate

فهرست مطالب
- ۱ خواص، ویژگیها و کاربردهای بی کربنات سدیم
- ۲ روشهای تولید سدیم بی کربنات
- ۳ خواص و کاربردهای جوش شیرین
- ۴ مشخصات فیزیکی و شیمیایی جوش شیرین، سدیم بی کربنات
- ۵ کاربردهای جوش شیرین در صنعت چیست؟
- ۶ فرق جوش شیرین صنعتی و خوراکی
- ۷ تفاوت جوش شیرین دامی و خوراکی
- ۸ ایمنی سدیم بی کربنات سدیم
- ۹ بسته بندی جوش شیرین
- ۱۰ خرید و فروش جوش شیرین، بی کربنات سدیم
خواص، ویژگیها و کاربردهای بی کربنات سدیم
جوش شیرین یا بی کربنات سدیم sodium bicarbonate چیست؟ سدیم بی کربنات (نام IUPAC :سدیم هیدروژن کربنات) که معمولاً به عنوان جوش شیرین یا بی کربنات سودا نیز شناخته میشود، یک ترکیب شیمیایی با فرمول NaHCO۳ است. این ترکیب، یک نمک معدنی است که از کاتیون سدیم (Na+) و آنیون بی کربنات (HCO۳–) تشکیل شده است.
جوش شیرین یک جامد سفید رنگ با ظاهر بلوری است اما اغلب به صورت یک پودر با دانهبندی ریز، به فروش میرسد. جوش شیرین، کمی شور مزه بوده و خاصیت نسبتاً قلیایی دارد. ترکیب معدنی حاوی این نمک در چشمههای آب شور و چشمههای معدنی یافت میشود.
نگاهی به تاریخچه جوش شیرین
جوش شیرین چیست؟ در سال ۱۷۹۱، شیمیدان فرانسوی به نام “نیکلاس لبلانک” توانست برای اولین بار، کربنات سدیم را تولید کند که به آن خاکستر سودا نیز می گویند. در سال ۱۸۴۶، دو نانوای آمریکایی، “جان دوایت” و “آستین چرچ”، اولین کارخانه تولید جوش شیرین از کربنات سدیم و دی اکسید کربن را در آمریکا تأسیس کردند.
بی کربنات سدیم توسط فردی به نام Rudyard Kipling در دهه ۱۸۰۰ معرفی شد؛ یک ترکیب که میتوانست در ماهیگیری تجاری استفاده شود تا از خراب شدن ماهی تازه صید شده جلوگیری کند. این کاربرد، گستردهترین موارد استفاده از سدیم بی کربنات در آن زمان بود.
در سال ۱۹۱۹، یک سناتور آمریکایی اعلام کرد که جوش شیرین میتواند آنفولانزای اسپانیایی را درمان کند! برخی از مطالعات آن زمان نشان داد که جوش شیرین چیست و چه اثرات درمانی برای بیماریهایی نظیر آنفولانزا دارد.

روشهای تولید سدیم بی کربنات
۱-تولید جوش شیرین در صنعت:
برای اینکه بهتر بدانید بی کربنات سدیم چیست لازم است با روش تولید این ماده آشنا شوید. بی کربنات سدیم به صورت صنعتی از کربنات سدیم تولید میشود:
Na2CO3 + CO2 + H2O →۲ NaHCO3
سودا اَش، استخراج شده به شکل سنگ معدن ترونا (Trona)، در آب حل شده و با دی اکسید کربن تیمار میشود. بی کربنات سدیم به صورت جامد از این محلول به صورت رسوب، خارج میشود.
در مورد فرآیند Solvay، بی کربنات سدیم، یک ترکیب واسطهای در واکنش کلرید سدیم، گاز آمونیاک و دی اکسید کربن است. با این وجود، این محصول، خلوص کمتری (۷۵ درصد) را دارد:
NaCl + CO2 + NH3 + H2O → NaHCO3 + NH4Cl
اگر چه ارزش تجاری و تولیدی قابل توجهی ندارد اما سدیم بی کربنات به دست آمده از واکنش دی اکسید کربن با محلول آبی هیدروکسید سدیم، نیز به دست آید:
CO2 + NaOH → NaHCO3
۲-تولید سدیم بی کربنات از طریق استخراج از معدن:
کانسارهای طبیعی ناکولیت (nahcolite) حاوی ترکیب معدنی بی کربنات سدیم هستند. این معادن در دوره ائوسن در زمان تشکیل رودخانه سبز در کلرادو ایجاد شدهاند. این رسوبات در طول زمان، در اثر تبخیر بستر رودخانه، به مرور ته نشین شدهاند. استخراج تجاری سدیم بی کربنات از این منطقه با استفاده از تکنیکهای معمول استخراج زیرزمینی مانند استخراج گودال، حفر درام و استخراج طولی مشابه استخراج ذغال سنگ انجام میشود.
مقادیر محدودی از محصول، با استخراج محلول سدیم بی کربنات از طریق پمپاژ آب گرم از بسترهای ناکولیت و بازیابی “ناکلیت” محلول در سطح زمین به دست میآید. این استخراج از طریق یک فرآیند تبلور با خنک کننده طبیعی انجام میشود.
خواص و کاربردهای جوش شیرین
sodium bicarbonate چیست؟ سدیم بی کربنات یک ترکیب آمفوتریک است. محلولهای آبی به دلیل تشکیل اسید کربنیک و یون هیدروکسید، نسبتاً قلیایی هستند.
بی کربنات سدیم میتواند به عنوان عامل شستشو دهنده برای از بین بردن هرگونه ناخالصیهای اسیدی از “مایعات خام” و تولید نمونه خالصتر استفاده شود. واکنش بی کربنات سدیم و اسید، یک نمک معدنی و اسید کربنیک تولید میکند که به راحتی به دی اکسید کربن و آب تجزیه میشود:
NaHCO3 + HCl → NaCl + H2CO3
H2CO3 → H2O + CO2
سدیم بی کربنات با اسید استیک (موجود در سرکه) واکنش میدهد و استات سدیم، آب و دی اکسید کربن تولید میکند:
NaHCO3 + CH3COOH → CH3COONa + H2O + CO2
بی کربنات سدیم با بازهایی مانند هیدروکسید سدیم واکنش داده و کربناتها را تشکیل میدهد:
NaHCO3 + NaOH → Na2CO3 + H2O
تجزیه حرارتی سدیم بی کربنات
در دمای ۸۰-۱۰۰ درجه سانتیگراد (۱۷۶-۲۱۲ درجه فارنهایت)، بی کربنات سدیم به تدریج به کربنات سدیم، آب و دی اکسید کربن تجزیه میشود. سرعت این تبدیل در دمای ۲۰۰ درجه سانتیگراد (۳۹۲ درجه فارنهایت) سریعتر است:
۲ NaHCO3 → Na2CO3 + H2O + CO2
با گرم شدن بیشتر، کربنات به اکسید تبدیل میشود (بالاتر از ۸۵۰ درجه سانتیگراد):
Na2CO3 → Na2O + CO2
مشخصات فیزیکی و شیمیایی جوش شیرین، سدیم بی کربنات
| نام ترکیب | |
| IUPAC نام گذاری سدیم هیدروژن کربنات/Sodium hydrogen carbonate |
|
| نامهای دیگر: جوش شیرین نانوایی- بی کَرب- بی کربنات سودا- ناکولیت |
|
| شاخصهای شناسایی | |
| ۱۴۴-۵۵-۸ | CAS Number |
| ۲۰۵-۶۳۳-۸ | EC Number |
| E500 | E number |
| ۵۱۶۸۹۲ | PubChem CID |
| ویژگیها و خواص | |
| NaHCO3 | فرمول شیمیایی |
| ۸۴.۰۰۶۶ g mol−۱ | جرم مولی |
| کریستالهای سفید | شکل ظاهری |
| بدون بو | بو |
| ۲.۲۰ g/cm۳ | دانسیته |
| تجزیه به سدیم کربنات از دمای ۵۰ درجه سانتی گراد | نقطه ذوب |
| ۶۹ g/L (0 °C) ۹۶ g/L (20 °C) ۱۶۵ g/L (60 °C) |
حلالیت در آب |
| ۰.۰۲ wt% استون ۲.۱۳ wt% متانول -در۲۲ °C نامحلول در اتانول |
حلالیت در در سایر مایعات |
| ویژگی ساختاری | |
| مونو کریستال | ساختار کریستالی |
| ترموشیمی | |
| ۸۷.۶ J/mol K | ظرفیت حرارتی (C) |
| ۱۰۱.۷ J/mol K | آنتروپی مولار (So۲۹۸) |
| −۹۵۰.۸ kJ/mol | آنتالپی استاندارد تشکیل (ΔfH⦵۲۹۸) |
| −۸۵۱.۰ kJ/mol | انرژی آزاد گیبس (ΔfG˚) |
| ترکیبات مرتبط | |
| سدیم کربنات/Sodium carbonate | آنیونها |
| آمونیوم بی کربنات/Ammonium bicarbonate پتاسیم بی کربنات/Potassium bicarbonate |
کاتیونها |
|
سدیم بی سولفات/Sodium bisulfate Sodium hydrogen phosphate/سدیم هیدروژن فسفات |
سایر ترکیبات مشابه |
کاربردهای جوش شیرین در صنعت چیست؟
۱-کاربرد سدیم بی کربنات در صنایع غذایی
بی کربنات سدیم، همان جوش شیرین یا کربنات هیدروژن سدیم است. از این ماده اولیه صنعتی در گرید خوراکی، به طور عمده در صنایع تهیه نان و شیرینی پزی استفاده میشود. میتوان از آن به عنوان ترکیب تهیه مایه خمیر، جوش در خمیر نان، محیط بافر (=تنظیم PH) استفاده کرد. موارد دیگر را در قسمت زیر مشاهده میکنید:
-
بی کربنات سدیم به عنوان ماده اولیه در تهیه بکینگ پودر:
برای افزایش حجم خمیر تهیه انواع نان، شیرینی، کیک، کراکر و ویفر، بکینگ پودر، ضروری است. بکینگ پودر شامل سه نوع ماده تشکیل دهنده اصلی است:
- یک عامل اساسی: سدیم بی کربنات
- یک عامل اسیدی: به عنوان مثال، سدیم اسید پیرو فسفات (SAPP) یا اسید سیتریک
- یک عامل حجم دهنده: برای مثال، نشاسته ذرت
نسبت استاندارد ۳۰/۴۰/۳۰ درصد وزنی (نشاسته / سدیم اسید پیرو فسفات / سدیم بی کربنات) است. به عمل آمدن خمیر مایه با آزاد شدن کربن دی اکسید همراه است. این واکنشها را در شکلهای زیر مشاهده میکنید:
دو واکنش شیمیایی (واکنش ۲a و ۲b):

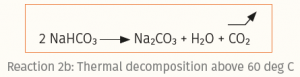
واکنش ۲a برای کربن دی اکسید، عملکرد بالاتری نسبت به واکنش ۲b دارد. واکنش ۲a هنگامی شروع میشود که معرفها در حین تهیه خمیر، حل شوند. واکنش ۲b، با گرم شدن، آغاز میشود.
میزان واکنش ۲a به پارامترهای مختلفی از جمله انتخاب ماده اسیدی و اندازه ذرات سدیم بی کربنات بستگی دارد. بی کربنات سدیم با ذرات بزرگتر، زمان انحلال بیشتری نسبت به ذرات ریزتر دارد (جدول زیر را مشاهده کنید)، بنابراین در سرعت واکنش تأثیر دارد. سرعت واکنش برای ذرات بزرگتر، کندتر از ذرات ریزتر است.
با این حال باید توجه داشت که ممکن است در صورت وجود بیش از حد بی کربنات سدیم، یک واکنش غیر مطلوب رخ دهد. (واکنش شکل زیر را مشاهده کنید).
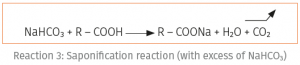
این یک واکنش صابونی شدن بین سدیم بی کربنات و اسید چرب آزاد موجود در فرمولاسیون است (اسید چرب که از موادی مانند کره یا خامه حاصل میشود). این واکنش، یک نمک اسید چرب تولید میکند که طعم ناخوشایند، شبیه به طعم فلزی را در مواد پخته شده ایجاد میکند.
-
جوش شیرین به عنوان بافر PH در صنایع غذایی:
بی کربنات سدیم میتواند به عنوان بافر pH استفاده شود؛ به این معنی که میتواند pH محلول را تنظیم و حفظ کند.
با چنین ویژگیای، برخی فرمولاسیونهای مواد غذایی، حاوی بی کربنات سدیم به عنوان بافر pH هستند. انواع رشته فرنگی آماده طبخ و همچنین نوشیدنیهای انرژی زا و قهوه یا چای آماده حاوی این ترکیب هستند.
به این ترتیب، استفاده از بی کربنات سدیم، دو فایده اصلی دارد. اولین مورد، کنترل بهتر pH محصول نهایی است به طوری که ثبات و ماندگاری محصول خوراکی بهتر را امکان پذیر میسازد.
بی کربنات سدیم، pH را تنظیم میکند و از ایجاد یک محیط اسیدی که باعث تکثیر باکتریها میگردد، جلوگیری مینماید. ثانیاً، سدیم بی کربنات در هنگام هضم، احساس بهتری در فرد ایجاد میکند.
-
سدیم بی کربنات عامل ایجاد “کف یا گاز” در مواد غذایی:
واکنش شیمیایی که در تولید کف یا جوش در تهیه نان یا کیک اتفاق می افتد، همان واکنش ۲a است که در قسمت قبلی به آن اشاره کردیم. بی کربنات سدیم و یک عامل اسیدی با هم واکنش میدهند تا کربن دی اکسید، آزاد کنند.
این خاصیت، برای فرمولاسیون نوشیدنیهای گازدار استفاده میشود. از اثر این واکنشها است که دی اکسید کربن محلول در نوشابهها به عنوان حباب گاز آزاد میشود.
از این ویژگی جوش برای تولید کف در نوشیدنیهای پودری مانند کاپوچینو یا نوشیدنیهای انرژی زا پودری نیز استفاده میشود. این واکنش زمانی اتفاق می افتد که پودر با آب مخلوط شود.
جوش شیرین پودری، زمان انحلال سریعتر در آب دارد و کف قوی با اثر سریع جرقهای تولید میکند. برعکس؛ ذرات بزرگتر، زمان انحلال طولانیتری دارند و کف ضعیفتری تولید میشود.
۲-کاربردهای صنعتی سدیم بی کربنات
– بدن انسان برای سلامتی به محدوده pH معینی نیاز دارد. وقتی ماهیت اسیدی، بیش از حد در هر یک از سیستمهای بدن ایجاد شود، آمپول بی کربنات سدیم یا قرص سدیم بی کربنات میتواند به سرعت با تشکیل یک واکنش اسید / باز، با افزایش PH بدن، مقابله کند. بیماریهای مزمن کلیه، سوزش معده، سنگهای کلیوی، افزایش اسید اوریک و اسیدوز متابولیک، همه با بی کربنات سدیم قابل درمان هستند.
– بی کربنات سدیم به طور مؤثر، دندانها و لثهها را تمیز میکند و اسیدیته طبیعی دهان را کاهش میدهد. اگر اسیدیته دهان، بالاتر از حد طبیعی باشد میتواند باعث عفونتهای دهانی شود. بنابراین، بسیاری از خمیر دندانهای بدون فلوراید، حاوی سدیم بی کربنات هستند.
– ۲۵ درصد از مقدار کل جوش شیرین دامی مورد استفاده در سراسر جهان به عنوان افزودنی خوراک دام استفاده میشود.
– در رنگرزی پشم، ابریشم و چرم از بی کربنات سدیم گرید صنعتی استفاده میشود.
– در صنایع تولید پلاستیک و پلیمرهای پیچیده از بی کربنات سدیم به عنوان تصفیه کننده و کاتالیزور استفاده میگردد.تجزیه بی کربنات سدیم باعث آزاد شدن دی اکسید کربن میشود؛ به طور چشمگیر از این ویژگی در تولید لاستیک و پلاستیک استفاده میشود.
– در حین پختن نخود فرنگی یا سایر سبزیجات، بی کربنات سدیم اضافه میگردد تا این سبزیجات، نرمتر شوند.
– مخلوط جوش شیرین و زیتون باعث نرمی و تردی بافت زیتونها میشود.
– جوش شیرین در مواد اولیه گل حفاری نیز کاربرد دارد.
– اکثر محصولات برطرف کننده لک صورت، حاوی جوش شیرین به عنوان یک ماده اولیه در فرمولاسیون هستند.
– بی کربنات سدیم، بوی سولفید موجود در تصفیه خانههای فاضلاب را کنترل میکند. همچنین با رشد بیولوژیکی میکروارگانیسمها مقابله میکند.
– به دلیل افزایش pH، قلیائیت مناسب آب با سدیم بی کربنات، هنگام تصفیه، حفظ میشود.
– از نظر شیمیایی، بی کربنات سدیم برای گوگرد زدایی در مسیر دودکش خروجی، به کار میرود. این فرآیند، گازهای صنعتی را قبل از انتشار در جو، تصفیه میکند.
– خاصیت ضد عفونی کننده بی کربنات سدیم، موجب شده است در صنایع دارویی بسیار با ارزش باشد. این ترکیب با ضد عفونی کردن، باکتریها و قارچها را از بین میبرد.
– مدیران کتابخانهها و مجموعه داران کتاب میدانند که با پاشیدن بی کربنات سدیم، لا به لای صفحات کتاب، بوی کهنگی که در کتابهای آسیب دیده یا قدیمیتر است، از بین میرود.
– کپسولهای آتش نشانی خشک و حاوی مواد شیمیایی که در خانهها و مشاغل استفاده میشود حاوی سدیم بی کربنات برای مقابله با آتش سوزیهای ناشی از جریان الکتریکی است.
برای مطالعه بیشتر: اوره، خواص شیمیایی، روش های تولید و کاربرد های آن.
فرق جوش شیرین صنعتی و خوراکی
جوش شیرین یکی از مهم ترین ترکیبات شیمیایی است که در صنایع مختلف برای فرآیندهای گوناگون استفاده می شود. این ماده دارای ساختار کربنات سدیم است اما در دو گرید صنعتی و خوراکی، وضعیت کمی متفاوت است. با دانستن تفاوت جوش شیرین صنعتی و خوراکی، به مهم ترین کاربردهای آنها پی خواهید بود.
به طور کلی، جوش شیرین صنعتی ترکیبی از کربنات سدیم با فرمول Na2CO3 است که دارای خلوص و کیفیت کمتری نسبت به جوش شیرین خوراکی است؛ ناخالصی جوش شیرین معمولا شامل فلزات سنگین، آهن، کربنات سدیم و آرسنیک و کلر است. اما جوش شیرین خوراکی دارای خلوص و کیفیت بالاتری است.
این ترکیب در آب، محلول است و در فرآیندهای صنایع هر دو ماده دارای آنیون کربنات و کاتیون سدیم هستند.غذایی و دارویی بسیار کاربرد دارد. از جوش شیرین خوراکی در تولید نوشابه های گازدار و تهیه مایه خمیر و پودر کیک استفاده می شود.
جوش شیرین گرید صنعتی، برای تمیزکاری و از بین بردن لکه ها در صنایع به کار می رود. روی بسته بندی جوش شیرین، عبارت هایی نوشته شده که نشان می دهد گرید خوراکی است یا صنعتی. برای جوش شیرین خوراکی، عبارت food grade و برای گرید صنعتی، عبارت industrial grade روی کیسه ها وجود دارد.
تفاوت جوش شیرین دامی و خوراکی
جوش شیرین، ترکیب مهمی است که در صنایع غذایی، خوراک دام و موارد صنعتی بسیار استفاده می شود. این ماده که در خوراک دام استفاده می شود با ترکیبی که در صنایع غذایی به کار می رود.
هر دو در واقع ماده ای به نام بی کربنات سدیم هستند که با فرمول شیمیایی NaHCO3 نشان داده می شوند و هر دو دارای کیفیت و خلوص بالا هستند زیرا خوراک دام و حیوانات نیز به اندازه انسانها باید که مورد دقت و توجه قرار گیرند. در واقع این دو گرید تفاوت چندانی با هم ندارند!
فرق جوش شیرین دامی و خوراکی در نوع کاربرد آنها است. در برخی موارد، برای خوراک طیور، از جوش شیرین گرید خوراکی یا همان ترکیب بی کربنات سدیم استفاده می شود. اینکه در خوراک دام از کدام گرید این ماده باید استفاده کرد تفاوت چندانی ندارد اما متخصصین این حوزه با توجه به وضعیت سلامت و تغذیه حیوانات و پرندگان این موضوع را تعیین میکنند.
ممکن است لازم باشد بی کربنات سدیم به غذای طیور اضافه کرد تا بیماری آنها برطرف شود و هنگام تخمگذاری، ذخایر بدنی بیشتری داشته باشند.
استفاده از جوش شیرین گرید صنعتی، دامی و خوراکی، به نوع فرآیندها و محصول یا نتایج نهایی بستگی دارد. برای تشخیص جوش شیرین دامی باید به برچسب روی بسته بندی حتما توجه کنید. اگر واژه Feed Grade بر روی بسته بندی وجود داشته باشد نشان دهنده گرید خوراک دام بودن این محصول است.
ایمنی سدیم بی کربنات سدیم
- سدیم بی کربنات باعث تحریک چشمها و پوست میشود. اگر از طریق پوست جذب شود ممکن است مضر باشد. در صورت بلعیدن تصادفی، به احتمال زیاد، مضر خواهد بود؛ مهمترین اثر، تحریک دستگاه گوارش است.
- استنشاق غبارات این ترکیب جامد ممکن است باعث تحریک دستگاه تنفسی شود.
- آسیبهای مزمن ناشی از تماس طولانی مدت با این ماده معدنی شامل آسیب به کبد و کلیه است.
پایداری شیمیایی جوش شیرین:
کربنات هیدروژن سدیم، هنگام گرم شدن، تجزیه میشود. این ترکیب ممکن است در معرض هوای مرطوب یا آب هم تجزیه شود.
از تماس این ماده با مواد ناسازگار باید خودداری کرد. تولید گرد و غبار، در معرض گرمای بیش از حد، دمای بالاتر از ۵۰ درجه سانتیگراد (۱۲۲ درجه فارنهایت)، قرار گرفتن در معرض هوای مرطوب یا آب، عوامل ناسازگار برای این ترکیب هستند.
سدیم بی کربنات با سایر مواد نظیر عوامل اکسید کننده قوی، اسیدها، فسفات مونوآمونیوم، آلیاژهای سدیم و پتاسیم، ناسازگاری دارد.
محصولات خطرناک تجزیه شدن از این ترکیب شامل مونوکسیدکربن و دی اکسیدکربن است.
بسته بندی جوش شیرین
بسته بندی جوش شیرین ساچیبسته بندیهای سدیم بی کربنات، در کیسههای پلی اتیلن یا پلی پروپیلن با وزن ۲۵ کیلوگرم و ۵۰ کیلوگرم به همراه کاور شرینک و بر روی پالت و همچنین جامبوبگ ۱۰۰۰ کیلوگرمی وجود دارد.
بسته بندیهای کربنات سدیم مرک در وزن کمتر از ۱ کیلوگرم، به صورت متداول در وزن ۵۰۰ گرم عرضه میشوند. این محصول دارای گرید آزمایشگاهی بوده و تولید کشور آلمان است.

شرایط نگهداری سدیم بی کربنات
محیط نگهداری بستهها و کیسههای مخصوص سدیم بی کربنات باید از تهویه مناسب برخوردار باشد. تولید و تجمع گرد و غبار را برای این ماده به حداقل برسانید. سعی کنید این ترکیب با چشمها و پوست شما تماس نداشته باشد و اگر روی لباس شما تجمع یافت، سریعاً لباس خود را تعویض کنید و بشویید.
بسته بندیهای سدیم بی کربنات باید در جای خشک و خنک نگهداری شود و درب ظرف، محکم بسته شود.
خرید و فروش جوش شیرین، بی کربنات سدیم
سدیم بی کربنات یکی از متداولترین و پرمصرفترین ترکیبات شیمیایی صنعتی است. این ماده در گرید خوراکی و صنعتی و آزمایشگاهی در بازار وجود دارد. از گرید خوراکی این ترکیب میتوان به بی کربنات سدیم دارویی نیز اشاره کرد. بی کربنات سدیم در مواد غذایی، بسیار استفاده میشود. جوش شیرین با برندهای ساچی، پارس، معین کانساران توس و فجر پارسیان در بازار عرضه میشود.
قیمت جوش شیرین (قیمت بی کربنات سدیم)
قیمت جوش شیرین به عوامل مختلفی مانند خلوص، کیفیت، برند و مقدار آن بستگی دارد. برای اطلاع از قیمت دقیق جوش شیرین، میتوانید با فروشندگان مختلف تماس گرفته و استعلام قیمت بگیرید.
خرید و فروش جوش شیرین در بسته بندیهای مورد نیاز مشتری امکان پذیر است. برای دریافت قیمت روز و آشنایی با نحوه سفارش این ماده میتوانید به وبسایت “شیمیکو“ مرجع تجارت مواد شیمیایی صنعتی مراجعه فرمایید.
برخی از تولیدکنندگان عمده جوش شیرین در ایران
- شرکت صنایع شیمیایی فارس: این شرکت بزرگترین تولیدکننده جوش شیرین در ایران است و سالانه بیش از ۱۰۰ هزار تن جوش شیرین تولید میکند.
- شرکت پتروشیمی ارومیه: این شرکت نیز یکی از تولیدکنندگان بزرگ جوش شیرین در ایران است و سالانه حدود ۵۰ هزار تن جوش شیرین تولید میکند.
- شرکت شیمیایی دماوند: این شرکت نیز در زمینه تولید جوش شیرین فعالیت میکند و سالانه حدود ۲۰ هزار تن جوش شیرین تولید میکند.
- شرکتهای دیگر: علاوه بر شرکتهای ذکر شده، شرکتهای دیگری نیز در زمینه تولید جوش شیرین در ایران فعالیت میکنند که از جمله آنها میتوان به شرکتهای شیمیایی کیمیا پارس شایانکار، شیمیایی رازی، شیمیایی صدف و شیمیایی باختر اشاره کرد.
 تأمین کنندگان ایرانی بی کربنات سدیم
تأمین کنندگان ایرانی بی کربنات سدیم
منابع:
https://en.wikipedia.org/wiki/Sodium_bicarbonate
https://www.bellchem.com/news/the-many-uses-of-sodium-bicarbonate
آخرین دیده شده ها














 (10 امتیاز)
(10 امتیاز)

دیدگاه کاربران
مفید بود. متشکرم
مطالب مفیدی بود؛ متشکرم.
متشکرم
سلام
امیر بخت همت هستم از کویت
قیمت سدیم بی کرنات در جامبو بک تا خرمشهر را لطفااعلاکنید
سلام و درود
خواهشمند است آگهی خرید خود را منتشر کنید یا در صورت نیاز به راهنمایی با شماره ۰۲۱۸۸۹۹۰۵۷۹ تماس حاصل فرمایید.
با تشکر
باسلام و عرض ادب
سوالی داشتم خدمتون
جوش شیرین صنعتی به چه نسبتی در آب حل میشود؟ و در چه دمایی؟
باتشکر
با سلام و احترام
در جدول مشخصات فیزیکی و شیمیایی به میزان حلالیت اشاره شده است.
باسلام و عرض ادب
لطفا تفاوت بین جوش شیرین گرید خوراکی و صنعتی به طور مختصر توضیح دهید. باتشکر فراوان
ایا جوش شیرین به دو دسته خوراکی و غیر خوراکی تقسیم بندی شده است ؟
سلام و درود
بله جوش شیرین در دو گرید خوراکی و صنعتی وجود دارد و مورد استفاده قرار میگیرد.
سود پرک چیست؟ همه چیز درباره سود سوز آور
آدیپیک اسید چیست و چه کاربردهایی دارد؟
کاربردهای آنتی اکسیدان ۱۰۱۰ چیست؟
نگهداری مواد شیمیایی در انبار استاندارد دارای چه ویژگی هایی است؟
آشنایی با طبقهبندی مواد خطرناک (IMDG Code)
با مواد اولیه بازیافت، مراحل بازیافت و نکات مهم آن آشنا شویم
شرکت پرسال تامین کننده اسید فسفریک خوراکی
هیدرازین چیست؟ روش تولید، ۲۳ کاربرد هیدرازین
مواد اولیه نساجی و مواد شیمیایی مورد استفاده آن چه هستند؟
کاربردهای اسیدهای شیمیایی در صنایع غذایی
چگونه از خاکستر برای تغذیه و تقویت گیاهان خود استفاده کنید؟
کاربرد کلروپتاس در گل حفاری چیست؟
سود پرک چیست؟ همه چیز درباره سود سوز آور
۱۰ روش موثر برای باز کردن لوله فاضلاب سینک ظرفشویی با ترفندهای خانگی
بیست و هشتمین نمایشگاه بین المللی نفت، گاز، پالایش و پتروشیمی
۳۱امین نمایشگاه بینالمللی ایران بیوتی
دومین نمایشگاه و کنفرانس پتروتک
نکات کلیدی در انتخاب بهترین کود برای گیاهان آپارتمانی
نمایشگاه بینالمللی عرب پلاست
نمایشگاه بینالمللی ایران کانمین
چهاردهمین نمایشگاه بینالمللی ایران نانو
هفدهمین نمایشگاه بینالمللی ایرانپلاست ۲۰۲۳
همه چیز درباره رزینها | انواع رزین و کاربرد آنها
کافئین چیست و چه اثراتی بر بدن دارد؟ – روش تولید تجاری کافئین